Avances
BENEFICIO CLÍNICO
FDA aprueba nuevo tratamiento que muestra resultados efectivos para ralentizar el Alzheimer
El nuevo medicamento frena un 27 por ciento el deterioro cognitivo leve
Viernes, 07 de julio de 2023, a las 14:58
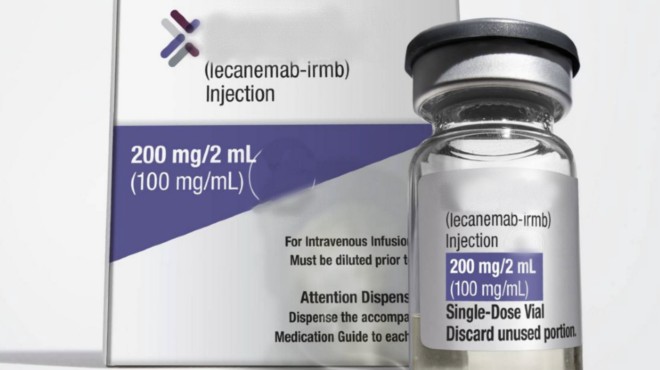
El fármaco aprobado por la entidad ralentiza la progresión de Alzheimer. |
Redacción. Bogotá
La Administración de Alimentos y Medicamentos de Estados Unidos (FDA por sus siglas en inglés) ha aprobado un nuevo tratamiento para el Alzheimer, un medicamento que ha mostrado resultados efectivos para tratar la enfermedad.
De acuerdo con un comunicado, la FDA ha explicado que, el compuesto de lecanemab ralentiza el deterioro cognitivo en la enfermedad de Alzheimer al reducir el depósito de beta amiloide cerebral.
“Leqembi es el primer anticuerpo dirigido contra la proteína beta-amiloide que pasa de un proceso de aprobación acelerada a uno de aprobación tradicional para el tratamiento de la enfermedad de Alzheimer. El medicamento funciona al reducir las placas amiloides que se forman en el cerebro, una característica fisiopatológica distintiva de la enfermedad”, ha apuntado en el informe.
El proceso se ha efectuado en un ensayo con 1,795 participantes, en el cual el nuevo compuesto ha demostrado frenar en un 27 por ciento el deterioro cognitivo en personas con Alzheimer o deterioro cognitivo leve en 18 meses.
De ese modo, este logro ha marcado el comienzo de una nueva era de tratamientos contra el Alzheimer, la forma más común de demencia, según los investigadores.
Es la primera vez que se confirma que un fármaco que ataca el proceso patológico subyacente del Alzheimer muestra beneficios clínicos. Un estudio confirmatorio ha verificado que es seguro y efectivo para pacientes con esta enfermedad, según informes oficiales.
Aunque la FDA ha otorgado la aprobación acelerada en enero, ahora se ha concedido la aprobación formal después de pasos adicionales. El Comité de Seguridad y Farmacología de la FDA respaldó por unanimidad los beneficios que permitirán modificar la progresión de la enfermedad.
El medicamento, desarrollado por Eisai y Biogen, es un anticuerpo monoclonal que elimina la proteína beta amiloide del cerebro, un marcador de la enfermedad de Alzheimer. Aunque se han reportado efectos secundarios graves en casos raros, la FDA ha emitido una advertencia y requiere un diagnóstico confirmatorio estricto.
Sin embargo, algunos críticos señalan que el medicamento tiene un efecto limitado y su impacto en la vida diaria de las personas es cuestionable. Además, su eficacia se limita a las primeras etapas de la enfermedad, lo que excluye a muchos pacientes debido a la falta de detección temprana.
Se espera que los programas federales de Estados Unidos amplíen la cobertura del medicamento, permitiendo el acceso a hasta un millón de personas con formas tempranas de la enfermedad.